溶解度参数怎么求(溶解度与溶解速度)
概 述
药物的溶解度和溶解速度在药物制剂的设计、 制备、质量控制中具有重要的意义,也是直接影响药物体内吸收与生物利用度的重要因素。在液体制剂 中,特别是多溶质溶液剂中,有必要了解溶质的溶解特性及一般药用溶剂的性质。
药物的溶解度和溶解速率是选择溶剂、制备均相和非均相液体制剂时需要关注的首要问题。每一种药物在一定的溶剂中均有各自的溶解度,许多药物在常用溶剂中的溶解度已被收载在药典中或其他参考书中。
溶解度
溶解度(solubility)系指在一定温度与压力下,物质在其饱和溶液中的浓度,即为物质在一定溶剂中的溶解度。溶解度是反映药物溶解性的重要指标。
溶解度常用一定温度下100g溶液(或100ml溶液)中溶解溶质的最大克数来表示。也可用物质的摩尔浓度 mol/L表示。各国药典一般用一定温度(多为25℃)下1g药物溶于若干ml溶剂来表示相对溶解度。

药物的溶解度分为特性溶解度和平衡溶解度。特性溶解度(intrinsic solubility)是指物不含任何杂质,在溶剂中不发生解离或缔合,也不发生相互作用时所形成的饱和溶液的泌度。特性溶解度是药物的重要物理参数之一,尤其是对新化合物而言更有意义.实际工作中,要完全排除药物解离和溶剂的影响是不易做到的。所以,一般情况下测定的溶解度多为平衡溶解度(equilibrium solubility),也称表观溶解度(apparent solubility)。
影响药物溶解度的因素
1、分子结构 药物在溶剂中的溶解度是药物分子与溶剂分子间相互作用的结果。若药物分子间的作用力大于药物分子与溶剂分子间的作用力,则药物 的溶解度小;反之,则溶解度大。
为了增加药物的溶解度,可将有机弱酸、弱碱药物制成可溶性盐,如将生物碱加酸制成可溶性盐类,可增加其在水中溶解度。在难溶性药物分子中引人亲水基团,可增加其在水中的溶解度。如维生素K3,不溶于水,分子中引入-SO3HNa,维生素K3,亚硫酸氢钠可制成水溶性注射剂。
2、多晶型 同一化学结构的药物,由于晶型不同,导致晶格能不同,药物的溶解度、溶解速度也不同。而无定形药物,因无晶格束缚,溶解度和溶解速度较结晶型大。例如维生素B2有三种晶型,在水中溶解度分别为:I型,60mg/L;II型,80mg/L;Ⅲ型,120mg/L.因此,可选择溶解度大的药物晶型制备液体制剂,并在制备和贮存过程中防止晶型的转变。
3、粒径 难溶性药物的粒径大于2000nm时,粒径对溶解度几乎无影响,但粒子小于100nm时,溶解度随粒径减小而增加。Ostwald-Freundlich 方程描述了难溶性药物的溶解度与粒径之间的定量关系。因此,可通过减小粒径至一定范围内来增加难溶性药物的溶解度。
4、溶剂化作用 药物在结晶过程中,溶剂分子进入药物晶格形成溶剂化物。由于结晶结构的改变而影响晶格能,在多数情况下,药物的溶解度和溶解速度按水合物<无水物<有机化物的顺序排列。例如琥珀酸磺胺嘧啶水合物的溶解度为100mg/L,无水物溶解度为390mg/L,戊醇溶剂化物溶解度为800mg/L。
5、温度 温度是决定药物溶解度和制备溶液时的一个重要因素。温度对溶解度的影响取决于溶解过程是吸热(△AHs>0),还是放热(△AHs<0)。当△ahs>0时,溶解度随温度升高而升高;如果△AHs<0时,溶解度随温度升高而降低。
溶解度与温度关系式为:
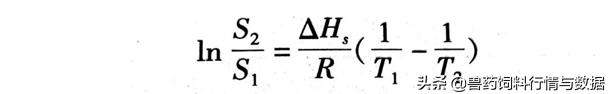
式中,S1,S2分别为温度T1和T2下的溶解度;△AHs为溶解焓,J/mol;R为摩尔气体常数。若已知溶解焓△AH.与某一温度下的溶解度S1,则可由式(2-1)求得T2下的溶解度S2。一般情况下,药物的溶解是一个吸热过程,因此,升高温度有利于增大药物的溶解度。
6、pH 多数药物为有机弱酸、弱碱及其盐类,这些药物在水中溶解度受pH影响很大。若已知药物的pKa和特性溶解度S0,对于弱酸性药物,可由式(2-2)计算不同pH下的表观溶解度S,亦可求得药物开始沉淀析出时的pH,以pHm表示,即溶液pH 低于pHm时,弱酸性药物游离析出。
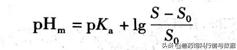
对于弱碱性药物,可由式计算表观溶解度S、pHm溶液pH高于pHm时,弱碱性药物游离析出。
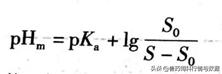
因此,对于有机弱酸、弱碱类药物,溶液的pH对药物的溶解度影响较大。
7、同离子效应 若药物的解离型或盐型是限制药物溶解的组分,则溶液中相关离子的浓度则可影响药物的溶解度。通常向难溶性盐类饱和溶液中加入含有相同离子的化合物时,其溶解度降低,称为同离子效应(common-ion effect)。如许多盐酸盐类药物在0.9%氯化钠溶液中的溶解度比在水中低。
增加药物溶解度的方法
液体制剂药物溶液的浓度取决于药物剂量和给药总量的要求。有些情况下,难溶性药物的溶解度不能够满足药物制剂浓度的要求,则需采取适宜的方法增加药物的溶解度。
增加难溶性药物溶解度的方法有加人增溶剂和助溶剂、使用混合溶剂、制成可溶性的盐、对药物的化学结构进行改造等。随着新理论、新技术的发展,增加药物溶解度的新方法也在不断出现。
1、加人增溶剂 增溶(solubilization)是指表面活性剂在水中形成“胶束”,增加难溶性药物在水中溶解度的过程。具有增溶能力的表面活性剂称为增溶剂。被增溶的物质称为增溶质。
每1g增溶剂能增加增溶质溶解的克数称为增溶量。用于口服制剂和注射剂所用的增溶剂大多属于非离子型表面活性剂,常用的有吐温类、聚氧乙烯蓖麻油等。如氯霉素在水中的溶解度为0.25%(W/W),加入20%吐温80后,溶解度可增大到50%(W/W)。
2.加入助溶剂 助溶(hydrotropy)系指难溶性药物与加入的第三种物质在溶剂中形成可溶性络合物、复盐或缔合物等,以增加药物在溶剂(主要是水)中的溶解度,这第三种物质称为助溶剂(hydrotropy agent) . 如碘在水中溶解度为 1:2950, 如加适量的碘化钾 ,可明显增加碘在水中溶解度,能配成含碘5%的水溶液,其中碘化钾为助溶剂,增加碘溶解度的机制是碘化钾(KI)与碘(I2)形成分子间的可溶性络合物 KI3。咖啡因与助溶剂苯甲酸钠形成苯甲酸钠咖啡因,溶解度由1:50增大到1:1.2。
常用的助溶剂表:

3、使用混合溶剂 为了提高难溶性药物的溶解度,常常使用两种或多种混合溶剂,在混合溶剂中各溶剂达到某一比例时,药物的溶解度出现极大值比在单纯溶剂中的溶解度都大,这种现象称潜溶(cosolvency)。
这种混合溶剂称为潜溶剂(cosolvent).如甲硝唑在水中的溶解度为10%(W/V),而在水-乙醇混合溶剂中,溶解度提高5倍。如苯巴比妥在90%乙醇中有最大溶解度。与水能形成潜溶剂的有乙醇、丙二醇、甘油、聚乙二醇等。
潜溶剂能提高药物溶解度的主要原因是:混合溶剂的介电常数、表面张力、分配系数等与溶解相关的特性参数发生了变化,使其与溶质的相应参数更相近的结果,这也遵循“相似相溶”的原理。
4、固体分散技术溶性药物与适宜载体可以形成固体分散体(solid dispersion),曲于载体材料的抑晶作用,此时药物以微晶态,无定形态、胶体分散态或分子分散态存在,具有很大的分散度,可增大药物的溶解度。如西沙必利-HPMC固体分散体,药物以无定型形式存在于固体分散体中,与西沙必利原料药相比,固体分散体中药物在人工胃液、水和人工肠中的溶解度分别提高了239.4%,132.6%和117.9%。
5、包合物技术 难溶性药物以分子状态被包裹于包合材料的空穴中,具有很高的分散性,从而使药物得到增溶。常用的包合材料为B-环糊精及其衍生物。如将难溶性药物槲皮素与羟丙基-B-环糊精制成包合物, 包合后槲皮素的溶解度由 0.0392mg/ml 增加到34.27mg/ml,溶解度提高了874倍。
溶解速度
溶解速度(dissolution rate)是指在一定温度下,单位时间药物溶解进人溶液主体的量,溶解速率取决于溶剂与溶质分子之间的引力及溶质分子在溶剂中的扩散速率。
药物的溶解过程包括两个连续的阶段,首先是溶质分子从固体表面溶解形成饱和层,然后在扩散作用下经过扩散层,再在对流作用下进入溶液主体内。固体药物的溶解速度主要受扩散控制,可用Noyes-Whitney 方程表示:
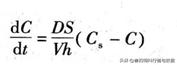
式中,dC/dt为溶出速度;D为溶质在溶出介质中的扩散系数;S为固体的表面积;V为溶出介质的体积;h为扩散层的厚度;Cs为溶质在溶出介质中的溶解度;C为t时间溶液中溶质的浓度。
影响药物溶解速度的因素
根据 Noyes-Whitney 固体的表面积、溶质在溶出介质中的溶解度及其扩散情况、溶出介质的体积等都会影响药物溶解速度。
1、固体的表面积 固体药物的粒径越小,孔隙率越大,表面积越大,药物的溶解速度越快。所以通过微粉化药物、加入润湿剂改善药物的分散度,有利于提高难溶性药物的溶解速度。
2、扩散系数 药物在溶出介质中的扩散系数越大,药物溶出速度越快。在温度一定的条件下,扩散系数大小受溶出介质的黏度和药物分子大小的影响。
3、扩散层的厚度 扩散层的厚度愈大,药物溶出速度愈慢。可通过搅拌,减小扩散层的厚度,加快药物溶出速度。
4、溶出介质的体积 溶出介质的体积小,溶液中药物浓度高,药物溶出速度慢;反之,则药物溶出速度快。
5、温度 温度升高,药物溶解度Cs增大,扩散增强,黏度降低,药物溶出速度加快。
,